گلیسرین با پتاسیم پرمنگنات
برای انجام این آزمایش Potassium Permanganate + Glycerin
حتما نکات ایمنی را رعایت کنید و حتی المقدور آنرا در زیر سقف انجام ندهید ویا یک ظرف آب در دسترس داشته باشید . واما متن علمی مربوط به این آزمایش با زبان اصلی از سایت زیر گرفته و نکات مربوط به آنرا در پست های بعدی خواهم گذاشت .
http://www.amazingrust.com/Experiments/how_to/KMnO4_Glycerin.html
Potassium Permanganate (KMnO4)
Potassium Permanganate (shown left) is a dark powder which, when dissolved in water, disassociates into K+1 and MnO4-1 ions to form a deep purple solution.
The Permanganate ion (MnO4-1) acts as an extremely powerful oxidizing agent in many chemical reactions.
Potassium Permanganate is such a powerful oxidizer, in fact, that when mixed with certain substances, a combustion reaction will proceed spontaneously without the need for a form of ignition.
When glycerin is poured onto a pile Potassium Permanganate powder, the Potassium Permanganate quickly begins to react, automatically starting a combustion reaction within seconds as shown in the video below.
Due to the intense heat liberated in the process, as well as the ease of starting the reaction, Potassium Permanganate / Glycerin is sometimes used to ignite thermite mixtures.
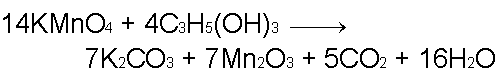



 مطالب وبلاگ در مورد فعالیت های گروه شیمی شهرستان قاین بوده و نقل واستفاده ازمطالب با ذکر منبع و ذکر آدرس وبلاگ بلا مانع می باشد .
مطالب وبلاگ در مورد فعالیت های گروه شیمی شهرستان قاین بوده و نقل واستفاده ازمطالب با ذکر منبع و ذکر آدرس وبلاگ بلا مانع می باشد .